CTC3.0:智能阅片(AI)+ 微量测序(SEQ)+ 细胞扩增 (in vitro culture)
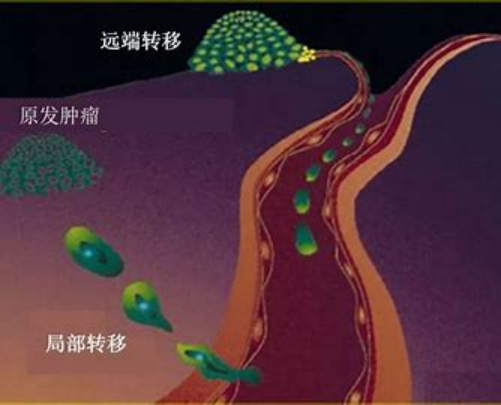
CTC是肿瘤血行转移的“种子”。
2004年,美国FDA批准强生公司“CellSearch®”上市,开启CTC临床应用新篇章。2013年,中国NMPA批准CellSearch®上市。
至今,CTC技术发展已历经三个时代。
CTC 1.0时代
FDA批准CellSearch®上市,计数EPCAM阳性上皮细胞,用于肠癌、乳腺癌和前列腺癌预后判断。国内外专家共识和指南把CTC作为肿瘤TNM外一个分期新指标。随2016年CellSearch®退市,“CTC1.0时代”黯然落幕。
CTC 2.0时代
重点聚焦CTC免疫表型和分子分型,用于靶向药物或免疫药物伴随诊断,迭代至“CTC2.0”。该类产品灵敏度显著提升,但整体操作复杂、周期长、重复性差,临床获益不足。虽有国内外指南或专家共识提及CTC意义,但临床使用范围仍然非常局限。
CTC3.0时代
通过AI扫描识别,CTC三合一分离技术大幅度提升检测效率,降低操作难度;CTC-NGS测序深度揭示转移细胞的分子信息;体外培养CTC,是耐药患者唯一的个性化体外试药机会,CTC应用拓展早诊、治疗、转移和复发的肿瘤全病程管理。
“CTC3.0”,度微医学新定义
—— 智能阅片 + 微量测序 + 细胞扩增
2023年,度微医学依据自主研发“尺寸过滤+阴性排除+阳性富集”CTC分离捕获仪CellSortingTM体系,具有"AI阅片+NGS测序+细胞扩增"三大技术特征。
领行业之先,度微医学以“人工智能阅片 + 微量细胞测序 + 体外细胞扩增”为核心特征的CTC3.0横空出世,CTC临床价值从辅助预后到伴随用药,正进入早诊、治疗和转移复发等肿瘤病程管理的全程。

至此,“CTC3.0时代”来临!
欢迎合作,请联系:15862368601 (微信同号),李先生
